AGENCIA EUROPEA DEL MEDICAMENTO
La EMA respalda la vacuna de Janssen tras hallar que su vinculación con los trombos es "muy rara"
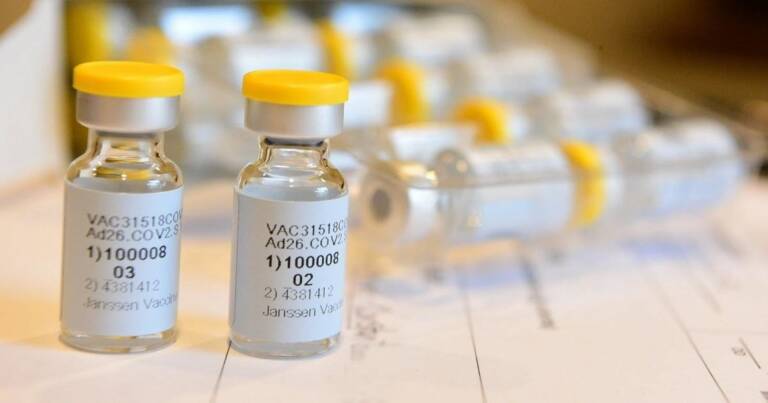
 FOTO: EUROPA PRESS
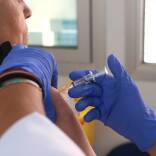
FOTO: EUROPA PRESSMADRID (EP). El comité de seguridad de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha concluido este martes que el beneficio-riesgo general sigue siendo positivo a la hora de administrar la vacuna contra la Covid de Jannsen, aunque confirma que se ha observado "un posible vínculo con casos muy raros" de coagulos sanguíneos inusuales relacionados con las plaquetas bajas en sangre, que serían los desencadenantes de los trombos.
Así, al igual que hizo hace dos semanas con la vacuna de AstraZeneca, el comité de seguridad de la EMA (PRAC, por sus siglas en inglés) concluye que se debe agregar una advertencia a la información del producto para la vacuna COVID-19 Janssen y que estos eventos deberían incluirse como efectos secundarios muy raros de la vacuna.
El pasado miércoles la compañía farmacéutica anunciaba que retrasaba el lanzamiento de su vacuna contra la COVID-19 en Europa, tras la paralización en Estados Unidos por los seis casos de eventos trombóticos en personas vacunadas con su inyección, tras administrar más de 6,8 millones de dosis de la vacuna.
Horas después la EMA señalaba que su comité de seguridad (PRAC, por sus siglas en inglés) estaba revisando también casos los seis trombos ocurridos en los Estados Unidos luego del uso de la vacuna COVID-19 de Janssen.
El tipo de coagulo de sangre informado, trombosis del seno venoso cerebral (CVST), se produjo en la mayoría de los casos en combinación con niveles bajos de plaquetas en sangre (trombocitopenia). Casos muy parecidos a los ocurridos con la vacuna de AstraZeneca, los cuales siguen en estudio desde la EMA, aunque ya hace dos semanas, tras un estudio preliminar, recomendó incluir estos acontecimientos adversos en la lista de efectos secundarios "muy raros" de la vacuna.
La vacuna COVID-19 Janssen es una vacuna para prevenir la enfermedad por coronavirus 2019 (COVID-19) en personas mayores de 18 años. Está compuesto por otro virus (de la familia de los adenovirus) que ha sido modificado para contener el gen para producir una proteína que se encuentra en el SARS-CoV-2. Destaca sobre el resto porque se administra en una sola inyección, aunque su eficacia es menor en comparación con el esto, del 67%. Consiguió la autorización de comercialización condicional por parte de la Comisión Europea el 11 de marzo de 2021.