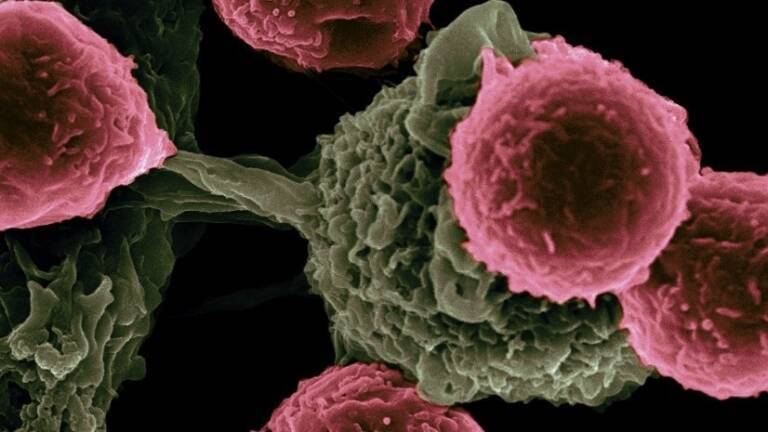
Dibujan el mapa del 'paisaje' inmune de los cánceres hematológicos para mejorar las terapias
 Foto: EP
Foto: EP MURCIA (EP). Investigadores de la Universidad de Helsinki y del Hospital Universitario de Helsinki, así como de la Universidad del Este de Finlandia, han dibujado el mapa del 'paisaje' inmune de las neoplasias hematológicas en un conjunto de datos que abarca a más de 10.000 pacientes para identificar objetivos farmacológicos y grupos de pacientes que podrían beneficiarse de las inmunoterapias.
Los tratamientos contra el cáncer que activan el sistema inmunitario han demostrado ser efectivos, particularmente en el caso de ciertos tumores malignos sólidos. Sin embargo, en el tratamiento de neoplasias hematológicas su potencial aún no se conoce completamente.
La reacción del sistema inmune del cuerpo contra el cáncer puede considerarse como un ciclo. Las células cancerosas contienen proteínas que difieren de las proteínas en otros tejidos. Sus componentes, conocidos como antígenos, deben ser presentados a las células T del sistema inmune por las células cancerosas.
Cuando identifican antígenos, las células T se activan y comienzan a destruir las células cancerosas, lo que hace que estas liberen más antígenos, mejorando aún más la respuesta inmune. Además de las células T, las células asesinas naturales (NK) tienen la capacidad de destruir las células. En inmunoterapias, el sistema inmune se activa terapéuticamente al impulsar diferentes etapas del ciclo.
En el estudio, publicado en la revista Cancer Cell, se utilizó un conjunto de datos que comprende más de 10.000 pacientes y varios cánceres hematológicos. Los investigadores estudiaron cómo los diferentes subtipos de cánceres hematológicos y las alteraciones genéticas de las células cancerosas están relacionados con las diferentes etapas de la respuesta inmune.
"El extenso estudio de las características inmunogenómicas de las neoplasias hematológicas realizadas en el estudio ayuda a los científicos y médicos a enfocar las inmunoterapias en los grupos de pacientes que obtienen el mayor beneficio, así como a comprender los factores que tienen un impacto potencial en la eficacia de las terapias", dice el profesor Satu Mustjoki, de la Universidad de Helsinki.
Ciertos subtipos de cáncer están asociados con una gran cantidad de células asesinas. Según los hallazgos, el citotóxico, que es tóxico para las células cancerosas, las células T y NK, es particularmente abundante en relación con ciertos subtipos de cáncer, como el linfoma de células B tipo B activado y la leucemia mieloide aguda, que tiene ciertas características genéticas del síndrome mielodisplásico. La investigación sobre tumores sólidos ha demostrado que grandes cantidades de células T y NK citotóxicas en el tejido tumoral dan como resultado una buena respuesta de inmunoterapia.
En el caso del mieloma múltiple, se produjo un número excepcionalmente alto de antígenos cancerosos, que potencialmente pueden usarse como objetivos de vacuna o terapia celular.
Las células cancerosas intentan esconderse de las células T al inhibir la presentación de antígenos a través de una variedad de mecanismos. Los investigadores encontraron que en ciertos subtipos de leucemia mieloide aguda, la metilación del ADN tenía una presentación de antígeno epigenéticamente silenciada.
Un fármaco que inhibe la metilación del ADN restableció la expresión de proteínas presentadoras de antígeno en pruebas de laboratorio. Como el medicamento ya se usa para tratar la leucemia mieloide aguda, podría aumentar potencialmente la eficacia de las inmunoterapias mediante el uso combinado.
"La clave del estudio fue la integración de la inmunología y el análisis computacional aplicado. Con la ayuda de métodos de análisis innovadores, pudimos correlacionar las características moleculares de las neoplasias hematológicas con la actividad de diferentes células inmunes", añade la profesora asociada Merja Heinäniemi, de la Universidad del Este de Finlandia.
El análisis de los datos y la interpretación de los resultados fueron realizados por Petri Pölönen, galardonado con el Premio al Investigador Joven de este año en la Universidad de Finlandia Oriental, y el estudiante de doctorado Olli Dufva de la Universidad de Helsinki.