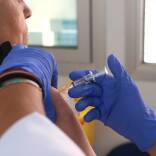
La EMA da el visto bueno al uso de la vacuna de Moderna en jóvenes de 12 a 17 años
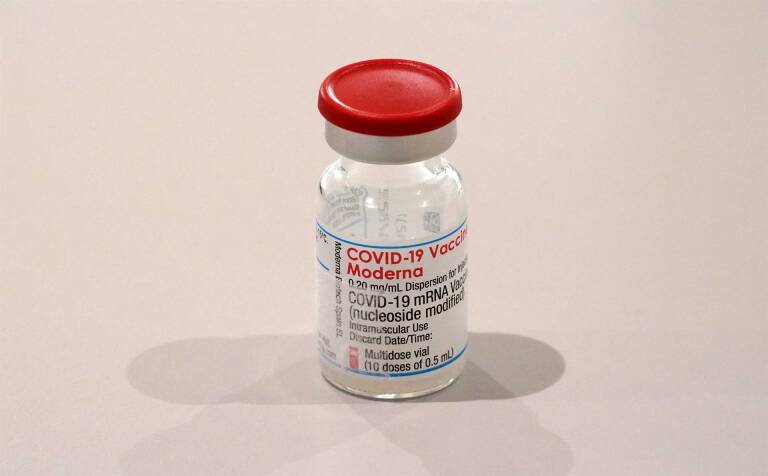
 FOTO: EUROPA PRESS
FOTO: EUROPA PRESSMURCIA. (EP) El Comité de Medicamentos de Uso Humano (CHMP, por sus siglas en inglés) de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha recomendado que se amplíe la indicación de la vacuna contra la COVID-19 de Moderna para incluir su uso en niños de 12 a 17 años. La vacuna ya está autorizada para su uso en personas de 18 años o más.
El uso en niños de 12 a 17 años será el mismo que en personas de 18 años o más. Se administra en dos inyecciones en los músculos de la parte superior del brazo, con un intervalo de cuatro semanas. Tras el dictamen positivo del CHMP, la Comisión Europea estudiará la posibilidad de autorizar la ampliación del uso de la vacuna.
Los efectos de la vacuna se han investigado en un estudio en el que participaron 3.732 niños de 12 a 17 años. El estudio demostró que Spikevax produjo una respuesta de anticuerpos comparable en niños de 12 a 17 años a la observada en adultos jóvenes de 18 a 25 años (medida por el nivel de anticuerpos contra el SARS-CoV-2).
Además, ninguno de los 2.163 niños que recibieron la vacuna desarrolló COVID-19, en comparación con cuatro de los 1.073 niños que recibieron una inyección ficticia. Estos resultados permitieron al CHMP concluir que la eficacia de la vacuna en niños de 12 a 17 años es similar a la de los adultos.
Los efectos secundarios más frecuentes en los niños de 12 a 17 años son similares a los de los mayores de 18. Incluyen dolor e hinchazón en el lugar de la inyección, cansancio, dolor de cabeza, dolor muscular y articular, aumento de los ganglios linfáticos, escalofríos, náuseas, vómitos y fiebre. Estos efectos suelen ser leves o moderados y mejoran a los pocos días de la vacunación.
El CHMP puntualiza, no obstante, que, debido al limitado número de niños y adolescentes incluidos en el estudio, el ensayo no podía haber detectado nuevos efectos secundarios poco comunes ni estimar el riesgo de efectos secundarios conocidos, como la miocarditis (inflamación del músculo cardíaco) y la pericarditis (inflamación de la membrana que rodea el corazón).
Sin embargo, resaltan que "el perfil de seguridad general determinado en adultos se confirmó en el estudio de adolescentes". "Por lo tanto, el CHMP consideró que los beneficios en niños de 12 a 17 años superan los riesgos, en particular en aquellos con condiciones que aumentan el riesgo de COVID-19 grave", detallan.
"La recomendación del CHMP de la autorización de nuestra vacuna para su uso en individuos de 12 años o más en la Unión Europea es un paso positivo hacia la autorización de nuestra vacuna en este grupo de edad. Mientras ayudamos a combatir la pandemia, esperamos poder contribuir a que los adolescentes vuelvan a la escuela de forma segura este otoño", ha comentado el director general de Moderna, Stéphane Bancel.
La vacuna de Moderna actúa preparando al organismo para defenderse del virus de la COVID-19. Contiene una molécula llamada ARN mensajero (ARNm) que tiene instrucciones para fabricar la proteína de la espiga. Esta es una proteína de la superficie del SARS-CoV-2 que el virus necesita para entrar en las células del organismo.
Cuando una persona recibe la vacuna, algunas de sus células leerán las instrucciones del ARNm y producirán temporalmente la proteína de espiga. El sistema inmunitario de la persona reconocerá entonces esta proteína como extraña y producirá anticuerpos y activará las células T (glóbulos blancos) para que la ataquen.
Si, más adelante, la persona entra en contacto con el virus del SRAS-CoV-2, su sistema inmunitario lo reconocerá y estará preparado para defender al organismo contra él. El ARNm de la vacuna no permanece en el organismo, sino que se descompone poco después de la vacunación.